注目の製品情報
2019/08/06
3次元細胞培養システム(AggreWell)における薬剤スクリーニングと表現型解析
- 用途別細胞培養
がん研究分野において、がんのin vivoにおける細胞間相互作用、微小環境や物質移動特性をより忠実に再現する、より生理的に適切な3次元のスクリーニングシステムへの移行の必要性が、一層認識されてきています。
いくつかの研究において、3次元のシステムは従来の培養法に比べてより薬物有効性を予測できることが示されています。しかし、生理的妥当性が高まると細胞培養作業や標準的な解析情報の複雑化を招き、不均一性が増加します。さらに、多くの3次元培養システムは労力や時間がかかり、得られる情報量が少ないものとなっています。
がんスフェロイドの3次元培養とスクリーニング利用の課題を克服するため、STEMCELL Technologies社のAggreWell™ プレートを使用した実験例をご紹介します。
研究概要
AggreWell™ プレートは、1回のピペッティングによってウェルごとにサイズ制御されたがんスフェロイドを大量に形成することができるマイクロウェルベースの3次元細胞培養プレートです(Figure 1)。画像化された各ウェル内において、すべてのスフェロイドを個別に特定し、指数化、解析を行なうことができます。これにより実験条件ごとに複数回繰り返し測定し、さらに代表的で予測的なデータを得ることができます。
実験方法
AggreWell™を使用して、がんのスフェロイド(MCF7 乳がん細胞株)を用いた3次元培養系による薬剤スクリーニングを実施しました。
AggreWell™400 24ウェルプレート (ST-34411) 内で無血清のMammoCult™ (ST-05620) 培地中に6x105個の細胞を播種することにより、500個のがんのスフェロイドの細胞を形成しました。播種から24時間後には、50%培地を交換することによってスフェロイドに薬剤処理を行ないました。MCF7細胞のこれら薬剤処理に対する感受性を評価するため、胸部組織に存在する管腔、基底部、乳腺上皮を標的とする薬剤化合物(Figure 2)を選択しました。各薬剤の50%効果濃度(EC50)範囲はタモキシフェン(TMX)濃度100 μM 、ラパチニブ(LTB)20 μM までの濃度範囲内でそれぞれ決定されました。DAPTは200 μM までは溶媒のみのものと比較して影響が出ることはありませんでした。複数の薬剤による処理を想定し、TMX 20 μM、LTB 5 μM、DAPT 10 μMで同時処理を行ないました。処理されたスフェロイドは画像を撮り、乖離させ、AO/DAPI 染色とNC-250 Nucleocounter (ChemoMetec)での解析によって生細胞を定量しました。各ウェル16個の個々のスフェロイドの形態学的パラメータは、ImageJにて解析しました。結果のデータセットは薬剤処理の影響を予測するパラメータを特定するために主成分分析(PCA)にて調査し、処置を分析し、要素を同定するためにグラフ化を行ないました。
Figure 2:乳がんの上皮細胞系列とそれらを標的とする薬剤
実験結果
Figure 3: 50%効果濃度(EC50)の決定と、対応するMCF7スフェロイドの形態学的変化
LTBやDAPTが(A)生存細胞ベースのEC50曲線や(B)処理後のスフェロイドにおける細胞生存の比較において中程度の影響度、もしくは全く影響がないのに対して、TMXはMCF7細胞株において最も一般的である管腔細胞を標的とし、細胞生存や細胞形態に最も大きく影響します。(C)TMX量依存的なE-カドヘリンの発現(緑)の変化により、細胞レベルで形態学的に変化が現れます。(D) TMX処理後における、AggreWell™プレート内のスフェロイドの代表的画像。EC50の濃度付近のTMX処理量ではスフェロイドの乖離がみられましたが、さらに高い濃度では直ちに起こってしまう細胞死のため形態学的変化を見ることはできませんでした。
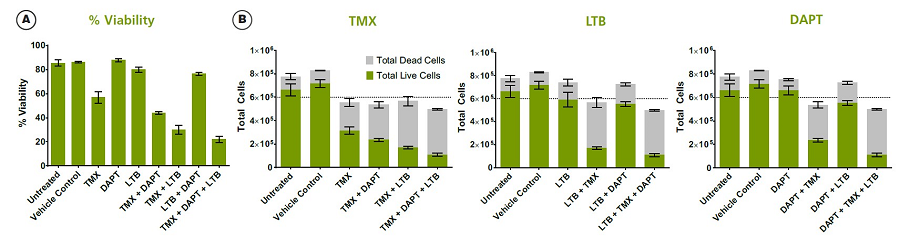
Figure 4: MCF7スフェロイドにおける多剤併用処理の相乗効果
LTBとDAPTは単独ではほとんど効果が見られませんが、TMXと併用することによって相乗的に作用して細胞生存を低下させます。これら3つを一緒に処理するとさらに細胞生存は低下します。単剤処理においてDAPTは作用がみられないため、併用処理によって細胞集団の一部においてDAPTに感受性になったことが示唆されます。データは(A)細胞生存率と(B)生細胞と死細胞それぞれの総細胞数として示されています。
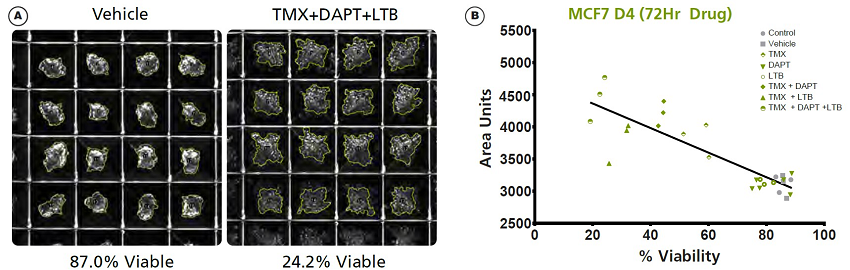
Figure 5:生細胞のパーセンテージとスフェロイドの形態の相関
(A)代表的画像の比較より、溶媒のみで処理したスフェロイド(Vehicle; 生細胞87.0%)と3つの薬剤で処理したスフェロイド(TMX+DAPT+LTB; 生細胞24.2%)間において、スフェロイドのサイズと形態には明らかな差異が見られました。(B)コントロール(Control)と溶媒のみで処理したスフェロイド(Vehicle)では生細胞が80%前後であるクラスタリングがしっかりした部分と、クラスタリングの程度が低い部分が見られます。薬剤で処理したスフェロイドでは測定領域(measure area)の増加につながるスフェロイドの乖離に伴い、細胞生存の低下が見られます。
Figure 6:薬剤処理の表現型マーカーの同定
(A)主成分分析(PCA解析)では、コントロール(Control)と3つの薬剤で処理した条件(Treatment)のクラスタリングはオーバーラップせず、各処理と強く関連した特徴を際立たせる固有ベクトルを有しています。そのため、将来の未知の化合物を検査するための処理条件の中から決定水準を定めるためにこれらのパラメータを使用することが可能です。(B) Aでハイライトされたパラメータのペアワイズ比較において選択されたプロットにより、処理群ごとの集団の分離を可視化することができます。
まとめ
AggreWell™はマイクロウェルベースの細胞培養システムであり、下記のような特長をもっています。
- 3次元のスフェロイド形成に有効なツールです
- 3次元培養系による薬剤スクリーニングを行なうための標準化されたプロトコールが確立できます
- 処理条件ごとに、同定と測定が可能な様々なスフェロイドを得ることができます
- 細胞ベースのアッセイによって、50%効果濃度(EC50)曲線や50%阻害濃度(IC50)曲線を決定することができます
文献
- Gangadhara et al. BMC Cancer, 16(1):345, 2016.
- Nath et al. Pharmacol Ther 163:93-108, 2016.